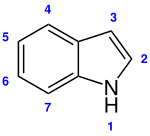
Indole
| Fórmula estrutural | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
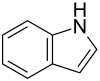
| ||||||||||||||||||||||
| Em geral | ||||||||||||||||||||||
| Sobrenome | Indole | |||||||||||||||||||||
| outros nomes |
|
|||||||||||||||||||||
| Fórmula molecular | C 8 H 7 N | |||||||||||||||||||||
| Descrição breve |
folhetos incolores puramente parecidos com flores e contaminados com um odor desagradável |
|||||||||||||||||||||
| Identificadores / bancos de dados externos | ||||||||||||||||||||||
| ||||||||||||||||||||||
| propriedades | ||||||||||||||||||||||
| Massa molar | 117,15 g mol −1 | |||||||||||||||||||||
| Estado físico |
firmemente |
|||||||||||||||||||||
| densidade |
1,22 g cm -3 (20 ° C) |
|||||||||||||||||||||
| Ponto de fusão |
52 ° C |
|||||||||||||||||||||
| ponto de ebulição |
254 ° C |
|||||||||||||||||||||
| Pressão de vapor |
1,6 Pa (25 ° C) |
|||||||||||||||||||||
| solubilidade |
pesado na água (3,56 g l -1 a 25 ° C) |
|||||||||||||||||||||
| instruções de segurança | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Dados toxicológicos | ||||||||||||||||||||||
| Tanto quanto possível e usual, unidades SI são usadas. Salvo indicação em contrário, os dados fornecidos aplicam-se às condições padrão . | ||||||||||||||||||||||
Indole é uma substância química a partir do grupo de aromáticos , heterocíclicos aminas e ocorre como um fragmento estrutural em muitos produtos naturais .
história
A química do indol começou com o estudo do amplamente utilizado corante índigo . O índigo pode ser convertido em isatina e posteriormente em oxindol . Em 1866, Adolf von Baeyer reduziu os oxindóis a indol com a ajuda do pó de zinco . Em 1869, ele propôs uma fórmula estrutural para o indol.
Certos derivados do indol foram corantes importantes até o final do século XIX. O interesse pelo indol aumentou na década de 1930 quando se tornou conhecido que o indol é um componente básico de muitas substâncias naturais importantes, como alcalóides (por exemplo, estricnina e auxina ) e o aminoácido triptofano e os neurotransmissores derivados dele ( serotonina , melatonina ). Continua a ser uma área de pesquisa ativa até hoje.
Ocorrência
O indol está contido no óleo de flor de jasmim , óleo de laca dourada , mas também nas flores de falsa acácia e arum . Em baixas concentrações, o indol dá o aroma floral típico e, portanto, também é adicionado aos perfumes . Em concentrações mais altas, o indol, como produto da degradação do aminoácido triptofano , junto com o escatol (3-metilindol), é a causa do fedor típico das fezes . Também está na ebulição a 240 a 260 ° C de alcatrão de carvão - fração contida.
O indol é parte do aminoácido proteinogênico triptofano .
apresentação
Indol ou derivados de indol podem ser representados de maneiras diferentes. Entre outras coisas, por meio de:
- Reação Japp-Klingemann
- Síntese de indol Bischler-Möhlau
- Síntese de indol de Larock
- Síntese de indol de Madelung
- Síntese de Leimgruber batcho indol
- Síntese de indol de Nenitzescu
- Síntese de indol de Gassman
- Síntese de reissert indol
- Síntese de indol de Fürstner
usar
Indol é o bloco de construção básico para corantes , hormônios e alcalóides . O corante mais conhecido derivado do indol é o índigo , mas o antigo corante roxo também é esse derivado . O bloco de construção indol é, entre outras coisas. no hormônio melatonina ( N -acetil-5-metoxitriptamina), no neurotransmissor serotonina (5-hidroxitriptamina) e na auxina ácido indol-3-acético . Os alcalóides que contêm indol incluem os alcalóides de estricnos (por exemplo, estricnina e brucina ), os alcalóides de cravagem ( ergotamina e seu derivado sintético LSD ) e o ingrediente de cogumelo psilocibina . Ele também é usado para fazer óleos artificiais de jasmim e neroli .
propriedades
O indol é fracamente básico, mas dificilmente forma sais com ácidos; em vez disso, ele reage prontamente para formar polímeros resinosos . O próton NH é abstraído por metais alcalinos . O anel pirrol reage preferencialmente em reações eletrofílicas . O indol inibe as enzimas quimiotripsina , lisozima e triptofanase .
prova
O teste do indol é usado na identificação de bactérias . Para fazer isso, adicione uma gota de dimetilaminobenzaldeído ( reagente de Ehrlich , reagente de Kovacs ) ao tubo MIO da série colorida , que fica vermelho cereja quando o triptofano é dividido em indol.
Derivados de indol
Existem numerosos derivados de indol que desempenham um papel na natureza (exemplo: triptofano ), tecnologia (exemplo: índigo ) e farmacologia (exemplo: indometacina ).
Links da web
Evidência individual
- ↑ Entrada no INDOLE no banco de dados CosIng da Comissão da UE, acessado em 30 de junho de 2020.
- ↑ a b entrada no indol. In: Römpp Online . Georg Thieme Verlag, acessado em 20 de junho de 2014.
- ↑ a b c d e f Entrada sobre indol no banco de dados de substâncias GESTIS do IFA , acessado em 8 de janeiro de 2018. (JavaScript necessário)
- ↑ Folha de dados indole (PDF) da Merck , acessada em 5 de setembro de 2016.
- ↑ Baeyer, A .: Sobre a redução de compostos aromáticos por meio de pó de zinco . In: Ann. . 140, 1866, página 295. doi : 10.1002 / jlac.18661400306 .
- ↑ Baeyer, A .; Emmerling, A.: Synthesis of Indole . In: Chemical Reports . 2, 1869, página 679. doi : 10.1002 / cber.186900201268 .
- ^ RB Van Ordem, HG Lindwall: Indole . Em: Chem Rev .. . 30, 1942, pp. 69-96. doi : 10.1021 / cr60095a004 .