Radiação de raios X característica
A radiação de raios X característica é um espectro de linha de radiação de raios X que surge nas transições entre os níveis de energia da camada interna de elétrons e é característica do respectivo elemento . Foi descoberto por Charles Glover Barkla , que recebeu o Prêmio Nobel de Física por ele em 1917 .
Emergência
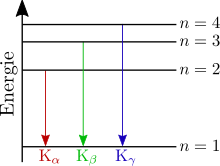
As linhas características do espectro de raios-X ( , ...) criado à imagem de modelo shell da seguinte forma:
- Um dos elétrons livres de alta energia do feixe de elétrons elimina um elétron que é ligado de acordo com a configuração do elétron na camada interna de seu átomo. Ao fazer isso, pelo menos tanta energia deve ser transferida para o elétron impactado quanto for necessária para saltar para uma camada ainda desocupada. Normalmente, a energia de impacto é maior do que a energia de ligação anterior do elétron e o átomo é ionizado .
- A lacuna resultante é fechada por um elétron de uma camada mais externa. Para fazer isso, o elétron de alta energia da camada localizada mais fora tem que desistir da diferença de energia ao mudar para uma camada localizada mais dentro. Ele emite um fóton (quantum de radiação).
A energia do fóton está normalmente na ordem de magnitude 1-100 keV correspondendo à diferença de energia da camada do elétron nos dois estados (elétron ausente na camada interna e na camada externa) e, portanto, está no espectro eletromagnético no X intervalo de raios. Os quanta de radiação, portanto, têm a diferença de energia entre a camada superior (por exemplo, L-) e inferior (por exemplo, K-). Como essa diferença de energia é específica do elemento, essa radiação de raios-X é chamada de radiação de raios-X característica .
O comprimento de onda e, portanto, a energia da radiação emitida podem ser calculados usando a lei de Moseley .
Designação das linhas espectrais
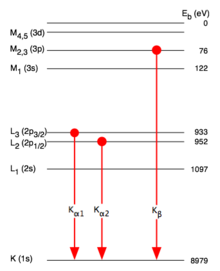
Para designar as linhas de raios-X, primeiro especifique a camada interna na qual o elétron passou durante a emissão, por exemplo, B. K, L, M etc. Uma letra grega como índice indica a diferença para o número quântico principal n da camada externa de onde o elétron veio. Por exemplo, corresponde a
- um índice um de 1, ou seja, H. a próxima camada superior (para a série K, esta é a camada L)
- um índice um de 2 (para a série K, esta é a camada M) etc.
Nas séries L e M e no caso de átomos com maior número atômico , essa atribuição não é mais tão clara. A divisão da estrutura fina desempenha um papel aqui. Além do índice grego, um índice numérico é usado para distinguir as linhas.
Aparecimento de várias linhas espectrais após uma excitação de elétrons
Os átomos com um número atômico mais alto têm várias camadas externas que podem fornecer um elétron para preencher o buraco na camada interna. O buraco também pode surgir em diferentes cascas internas. Conseqüentemente, esses átomos também podem emitir raios-X de diferentes energias.
- Depois de um elétron z. B. caiu da camada L para a camada K, a camada L está novamente com falta de pessoal. Outro elétron de uma camada ainda mais alta cai, emitindo outro fóton . Este segundo fóton é de menor energia e contribui para a linha L neste exemplo.
- Além da emissão de raios X - especialmente no caso de átomos leves com números atômicos - a transferência de energia para elétrons mais distantes é outra forma de compensar a diferença de energia (ver efeito Auger ).
Geração no tubo de raios X

Em um tubo de raios X , elétrons de alta energia atingem um ânodo e geram raios X característicos e bremsstrahlung . No espectro representado graficamente, as linhas dos raios X característicos aparecem como altas elevações ( picos ) no fundo contínuo do bremsstrahlung.
aplicativo
A radiação de raios-X característica é observada com detectores que determinam a energia ou o comprimento de onda dos quanta de raios-X. O espectro permite tirar conclusões qualitativas sobre a composição elementar da amostra, e uma correção ZAF também permite uma análise quantitativa. Este princípio é usado na análise de fluorescência de raios-X , dispersiva de energia (EDX / EDS) e espectroscopia de raios-X dispersiva de comprimento de onda (WDX / WDS).
Links da web
- Banco de dados (Banco de dados de energias de transição de raios X) para as energias dos raios X característicos (teóricos e experimentais) de várias substâncias
- LP: Radiação característica , Georg-August-Universität Göttingen. Notas, especialmente na notação.