Configuração de elétron
A configuração eletrônica indica a distribuição de elétrons em diferentes estados de energia e, assim, salas ( orbitais atómicas ) no âmbito do modelo de shell do shell atômica .
Números quânticos e cascas
O estado de cada elétron na camada é determinado por quatro números quânticos de acordo com o modelo atômico de Bohr-Sommerfeld e o modelo orbital :

| Número quântico | personagem | Faixa de valores | Descrição | Exemplos |
|---|---|---|---|---|
| Número quântico principal | 1, 2, 3, ... | K, L, M, ... | 3 | |
| Número quântico menor | 0, ..., n - 1 | s, p, d, f, ... | 0, 1, 2 | |
|
número quântico do momento angular magnético |
, ..., | s, p x, y, z , d yz, xz, xy, z², x²-y² , ... |
-2, -1, ± 0, +1, +2 | |
|
número quântico de spin magnético |
−½, + ½ | ↓, ↑ | −½, + ½ |
De acordo com o princípio de Pauli , dois elétrons de um átomo não devem ter o mesmo estado em todos os quatro números quânticos. Com este princípio, pode-se mostrar que os elétrons são distribuídos para os vários estados permitidos e, portanto, para as camadas e sub- camadas .
Os números quânticos principais determinam as camadas, os números quânticos secundários as sub-camadas. Cada camada, de acordo com as limitações de , e ser preenchida com no máximo 2n² elétrons. As camadas são designadas em ordem crescente, começando com a camada do núcleo, com letras maiúsculas: K, L, M, N, O, P, Q ... Os orbitais são nomeados de acordo com a série de linhas espectrais que um elétron excitado emite quando está no orbital original, cai para trás; Por razões históricas, as primeiras quatro séries são chamadas de s (“sustenido”), p (“principal”), d (“difuso”) ef (“fundamental”).
A camada mais externa ocupada ( camada de valência ) determina o comportamento químico e, portanto, é decisiva para a classificação na tabela periódica .
Encher as tigelas de acordo com o princípio de acumulação

Com um número crescente de elétrons nos elementos , os estados possíveis - começando com as energias mais baixas - estão ocupados. De acordo com a regra de Hund , os orbitais com a mesma energia são atribuídos primeiro uma vez, depois duas vezes.
As sub-camadas são preenchidas na seguinte ordem (em linhas, ou seja, em pontos):
- 1º período : 1s
- 2º período : 2s 2p
- 3º período : 3s 3p
- 4º período : 4s 3d 4p
- 5º período : 5s 4d 5p
- 6º período : 6s 4f 5d 6p
- 7º período : 7s 5f 6d ...
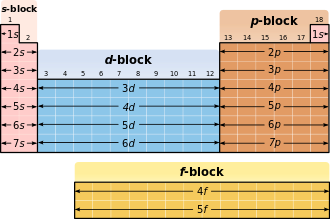
Relação com a tabela periódica
Na tabela periódica, a ocupação do orbital s de uma nova casca corresponde ao salto para um novo período .
| Orbital / bloco |
Número de elétrons |
inclui elementos de ... |
|---|---|---|
| s | 2 | Elementos do 1º e 2º grupo principal , bem como hélio |
| p | 6º | restantes elementos do grupo principal |
| d | 10 | todos os elementos do subgrupo |
| f | 14º | todos os lantanídeos e actinídeos |
notação
| 2p |
|
||||
|---|---|---|---|---|---|
| EU. | 2s |
|
|||
| K | 1s |
|
|||
| 1s 2 2s 2 2p 4 [He] 2s 2 2p 4 | |||||
A configuração eletrônica de um átomo é descrita pelas subcamadas ocupadas:
- O número da camada é seguido pela letra da camada inferior e sobrescrito o número de elétrons da camada inferior. Então, z. B. para a 2ª camada inferior (l = 1 ou p) da 3ª camada (n = 3 ou M) ocupada por 5 elétrons, a notação 3p 5 .
- Se houver vários subshells, o shell comum é omitido: 2s 2 2p 3 torna-se 2s 2 p 3 .
- No caso de outra notação abreviada, a abreviatura do gás nobre com o próximo número ordinal inferior é colocada entre colchetes, indicando as subcamadas ausentes do elemento a ser exibido.
Exemplo de cloro : 1s 2 2s 2 2p 6 3s 2 3p 5 → [Ne] 3s 2 3p 5 .
As subcamadas não devem ser especificadas de acordo com o princípio de construção, mas na ordem do número quântico principal; então z. B. para európio : [Xe] 4f 7 6s 2 .
Além disso, a célula ou notação de Pauling é comum como uma representação gráfica clara.